龙8long8,山东中医药大学: 整合生物信息学与实验验证解析黄芪-莪术药对抗肝
原发性肝癌是我国第4位常见恶性肿瘤及第2位肿瘤致死病因,其中约90%为肝细胞癌[1]。肝癌的发生、发展机制复杂,涉及多个原癌基因以及信号通路[2]。近年来,中药在肝癌的预防、控制转移与复发等方面所具有的优势,使其成为抗肝癌新药研发的热点和方向[3-5]。目前中医药界对于肝癌的理论及治疗研究逐渐增多,并形成了较为统一的认识,其病机在于气虚血瘀,其治法以益气活血为主[6]。黄芪-莪术是益气活血法代表性药对,源于张锡纯所著《医学衷中参西录》中的理冲汤,主治气虚血瘀证[7]。从中医理论讲,黄芪味甘性微温,可补气升阳,为“补中益气之要药”[8];莪术辛散苦泄,能破血散瘀,又能行气化积,是“破血化瘀之重药”[9];两药配伍使用“破中有补,补中有行,相得益彰”从而达到“补而不滞”之效,为益气活血配伍的典型代表[10]。孙桂芝教授擅用桃红芪术软肝煎起益气活血之效,认为黄芪-莪术配伍治疗肝癌时能够补脾胃、破癥消积,对肝癌有很好的抑制作用,在临床实践中运用此法与化疗联合使用,能够明显改善肝癌患者的生存质量,在提高肝癌远期疗效上具有一定优势[11-13]。黄芪-莪术药对配伍治疗肝癌的作用确切,在抗肝癌中药中具有重要地位,但是黄芪-莪术药对抗肝癌的配伍机制尚不明确。本研究整合生物信息学与网络药理学预测黄芪-莪术药对治疗肝癌的相关靶点和通路,将筛选得到的核心成分与靶点进行分子对接,探究黄芪-莪术药对的多成分、多靶点、多通路的配伍协同作用机制,并采用体外细胞实验对核心成分和靶点进行验证。系统研究黄芪-莪术药对抗肝癌配伍机制,不仅可为含有该药对的抗肝癌系列类方的研究提供参考,而且有利于指导中医临床的合理用药,同时为该类方的质量控制和新药研发提供重要的科学依据,为肝癌这一发病率日趋升高、严重威胁人类健康的重大疑难疾病治疗做出贡献。
2.1.3 黄芪、莪术化学成分收集及潜在活性成分筛选 在 TCMSP ( )数据库中对黄芪、莪术成分进行检索;将口服生物利用度( oral bioavailability , OB )≥ 30% 、药物相似性( drug-likeness , DL )≥ 0.18 的成分作为潜在活性成分,并结合文献报道,将具有体内外抗癌活性的黄芪、莪术成分补充到潜在活性成分中 [20-21] 。
2.1.4 黄芪、莪术活性成分靶点预测与抗肝癌靶点筛选 在 PubChem ( )数据库中检索“ 2.1.3 ”项下活性成分的 Isomeric SMILES 数据,将该数据输入 SEA ( )和 SwissTargetPrediction ( ) 2 个数据库,预测成分靶点,与 TCMSP 数据库中的靶点取并集得到潜在活性成分作用靶点,并在 Uniprot 数据库中对靶点基因名称进行校正,使蛋白质靶点信息标准化 [22] 。将成分作用靶点与“ 2.1.1 ”项下所筛选肝癌靶点取交集,得到黄芪、莪术抗肝癌靶点。
2.1.5 黄芪、莪术抗肝癌关键成分筛选 将“ 2.1.4 ”项下潜在活性成分靶点与“ 2.1.2 ”项下所筛选肝癌关键靶点取交集,采取疾病关键靶点“反向钩钓”关键潜在活性成分的方式,得到黄芪、莪术抗肝癌关键成分及其靶点。
2.1.7 拓扑网络构建与分析 采用 Cytoscape ( version 3.9.1 )软件构建肝癌关键靶点的 PPI 网络、成分 - 靶点网络、关键成分 - 靶点 - 通路网络。通过 Network Analyzer 插件对关键成分 - 靶点 - 通路网络的拓扑性质进行分析,获取成分、靶点、通路相关介数值。
2.1.8 黄芪、莪术抗肝癌核心成分及其抗肝癌核心靶点筛选 通过 1 种网络贡献指数( CI )评价黄芪 - 莪术抗肝癌成分发挥抗肝癌作用的贡献大小 [24] 。
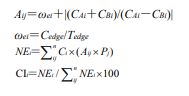
i 为成分的数量; j 为靶点的数量; ωei 为网络节点参数; Aij 为根据 ωei 值确定的亲和力指数; CAi 为黄芪关键成分 - 靶点 - 通路网络中每种抗肝癌成分的介数; CBi 为莪术关键成分 - 靶点 - 通路网络中每种抗肝癌成分的介数, Ci 为每种抗肝癌成分的介数; Pj 为每种靶点的介数,以参数由关键成分 - 靶点 - 通路网络中获得; NEi 为网络中 1 种抗肝癌成分的网络贡献; CI 为抗肝癌成分发挥抗肝癌作用的贡献大小
以“ hepatocellular carcinoma ”和“ liver cancer ”及活性成分的常用名称用作为关键词,检索 1990 — 2018 年出版于 PubMed 和 CNKI 数据库中的相关文献。如果前 N 个成分的 CI 总和超过 50% ,则认为这些相关的 N 个成分对黄芪和莪术发挥抗肝癌作用的贡献最大; CI 总和超过 90% ,则认为这些相关的 N 个成分对黄芪和莪术发挥抗肝癌作用的贡献最主要。核心成分在关键成分 - 靶点 - 通路网络中所调节的介数大于 5 的靶点为抗肝癌核心靶点。
2.1.10 核心基因在肿瘤及正常组织表达量差异分析 在癌症基因组图谱( cancer genome atlas , TCGA )网站中得到核心基因在肿瘤组织及正常组织中的表达量,进行差异表达分析 [25] 。
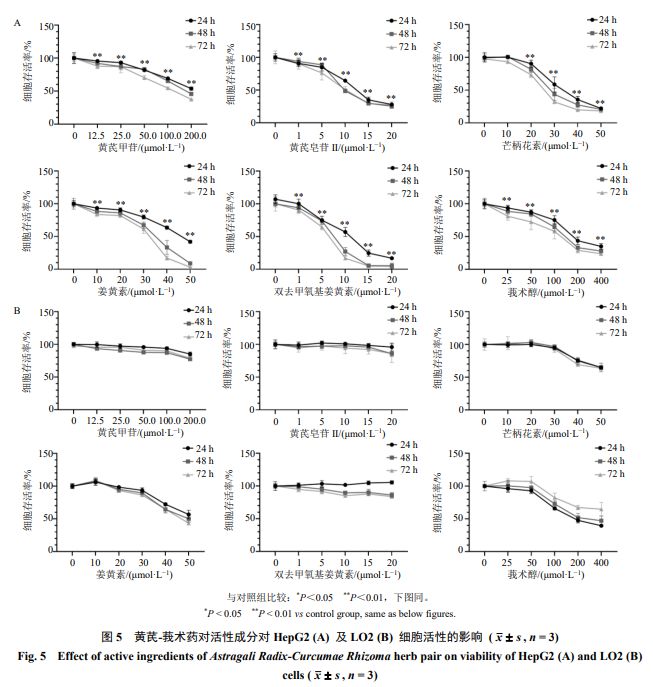
2.2.1 MTT 实验 将处于对数生长期的 HepG2 和 LO2 细胞分别以 5 000 个 / 孔接种到 96 孔板中,培养 24 h 后,分别给予不同浓度的黄芪皂苷 II 、黄芪甲苷、芒柄花素、莪术醇、姜黄素、双去甲氧基姜黄素,对照组加入不含药物的培养基,同时设置调零孔(不接种细胞),处理 24 、 48 、 72 h ,处理后每孔加入 10 μL MTT ( 5 mg/mL ), 37 ℃孵育 4 h ;去上清,加入 100 μL DMSO 终止孵育,使用酶标仪测定 570 nm 处的吸光度( A )值,计算细胞存活率 龙8long8。
2.2.2 药物协同作用研究 根据“ 2.2.1 ”项结果,从黄芪、莪术各成分中各选 1 个作用效果最佳的单体,进行药物协同作用研究。细胞存活率的结果通过 Chou-Talalay 模型进行分析,以评价黄芪 - 莪术成分配伍的协同作用,明确最佳协同剂量, CompuSyn 软件采用 Chou-Talalay 模型计算药物组合的组合指数,组合指数= 1 为加和效应,组合指数< 1 为协同作用,组合指数> 1 为拮抗作用 [24] 。
2.2. 4 Western blotting 法检测蛋白表达 选择“ 2.2.2 ”项单体对应的靶点在 Pymol 软件中进行分子对接可视化,并通过 Western blotting 实验验证单体对蛋白表达的影响。分组与给药同“ 2.2.3 ”项,收集药物作用后的 HepG2 细胞龙8long8,加入细胞裂解液提取总蛋白,使用 Nanodrop lite 检测蛋白浓度,蛋白样品经 10% 十二烷基硫酸钠 - 聚丙烯酰胺凝胶电泳,转至 PVDF 膜,经 5% 脱脂奶粉封闭后,加入一抗, 4 ℃孵育过夜;加入二抗, 37 ℃孵育 2 h ,使用 ECL 化学发光试剂盒显影,采用 Image J 软件分析条带灰度值。
2.2. 5 统计学分析 数据使用 Graphpad Prism 9.5 软件处理,采用单因素方差分析进行组间统计。
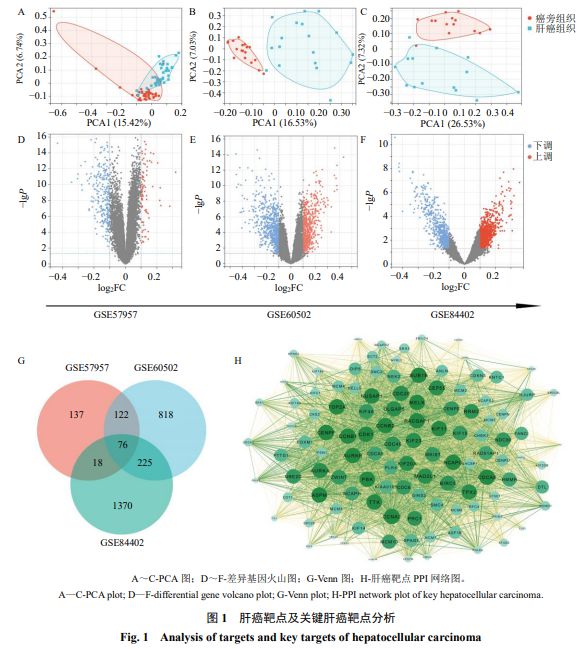
对 GSE57957 、 GSE60502 、 GSE84402 肝癌基因表达数据进行 PCA ,结果显示在 3 个数据集中,肝癌组织与癌旁组织基因表达均能明显区分(图 1-A ~ C );进一步 Limma 分析,结果显示在 3 组数据中 DEGs 分别有 353 个(上调 85 个,下调 268 个)、 1 241 个(上调 575 个,下调 666 个)、 1 689 个(上调 1 031 个,下调 658 个,图 1-D ~ F );将以上 3 组数据中的 DEGs 取并集,共得到肝癌靶点 2 766 个(图 1-G );进一步疾病关键靶点分析,结果显示 PPI 网络中得分最大为 97.33 的 MCODE 功能模块所含有的 112 个靶点为肝癌关键靶点(图 1-H )。
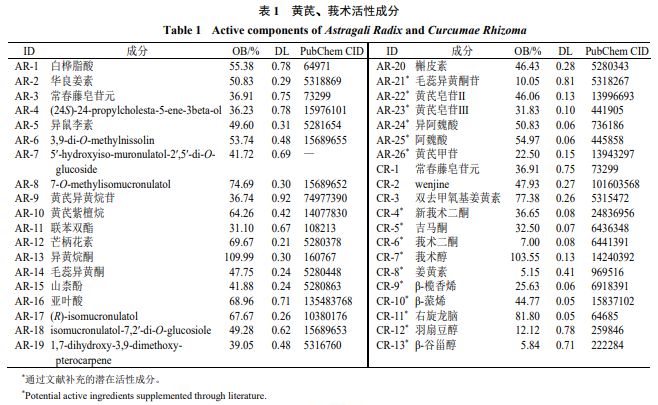
通过检索 TCMIP 数据库,得到黄芪化学成分 87 种,经筛选潜在活性成分 26 种,其中 OB ≥ 30% 、 DL ≥ 0.18 的成分 20 种( AR-1 ~ AR-20 ),通过文献补充的成分 6 种( AR-21 ~ AR-26 );得到莪术化学成分 81 种,经筛选潜在活性成分 13 种,其 中 OB ≥ 30% 、 DL ≥ 0.18 的成分 3 种( CR-1 ~ CR-3 ),通过文献补充的成分 10 种( CR-4 ~ CR-13 ),黄芪与莪术共有成分 1 种(常春藤皂苷元),共得到黄芪 - 莪术药对潜在活性成分 38 种(表 1 )。
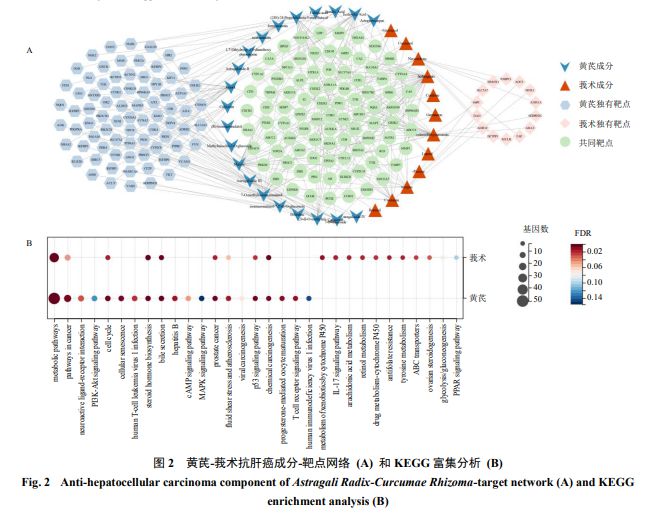
分别对黄芪 166 个靶点、莪术 103 个靶点进行 KEGG 富集分析,根据包含靶点数量筛选排名前 20 的通路,结果显示,黄芪与莪术所调节的 20 条通路中,共有通路有 9 条;其中黄芪中排名前 5 位的通路分别为代谢途径、癌症的通路、神经活性配体 - 受 体相互作用、磷脂酰肌醇 3- 激酶( phosphatidylinositol 3-kinase , PI3K ) - 蛋白激酶 B ( protein kinase B , Akt )信号通路、细胞周期,莪术中排名前 5 位的通路分别为代谢途径、癌症的通路、类固醇激素生物合成、胆汁分泌、化学致癌(图 2-B )。
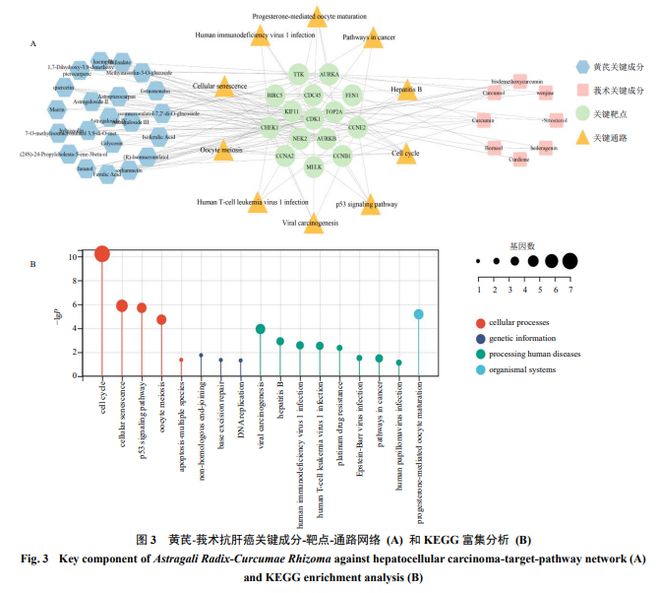
通过肝癌关键靶点进行“反向钩钓”,得到黄芪 - 莪术抗肝癌关键成分 29 种,其中黄芪抗肝癌关键成分 22 种、莪术抗肝癌关键成分 8 种,两者共有抗肝癌关键成分 1 种(常春藤皂苷元,图 3-A )。 29 种黄芪 - 莪术抗肝癌关键成分所调节抗肝癌关键靶点 15 个,对以上靶点进行 KEGG 富集分析,共得到 17 条通路,其中最为重要的细胞过程包含细胞周期、细胞衰老、 p53 信号通路、卵母细胞减数、细胞凋亡 - 多个物种共 5 条信号通路(图 3-B )。
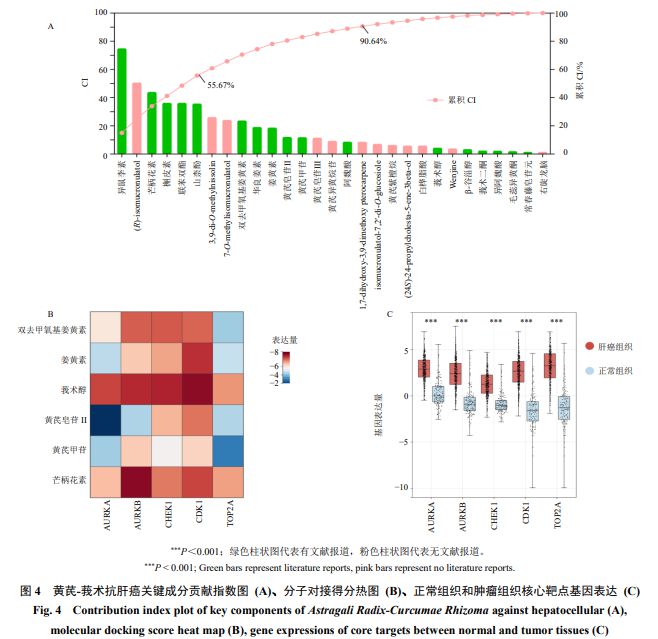
通过网络贡献指数模型,计算黄芪 - 莪术抗肝癌 29 种关键成分的抗肝癌作用贡献指数。根据计算结果, CI 值合计为 55.67% 的前 6 种成分均为黄芪成分,表明其抗肿瘤作用贡献最大; CI 值合计为 90.64% 的前 17 种成分中莪术成分有 2 种,在一定程度上表明黄芪 - 莪术配伍发挥协同抗肿瘤作用(图 4-A )。根据成分 CI 值及其所在中药中的相对特异性,选取黄芪中的黄芪皂苷 II 、黄芪甲苷、芒柄花素与莪术中的莪术醇、姜黄素、双去甲氧基姜黄素共 6 种成分作为黄芪 - 莪术药对的核心代表性成分,与之相对应的 CDK1 、 DNA 拓扑异构酶 2A ( topoisomerase 2A , TOP2A )、极光激酶 B ( aurora B , AURKB )、检查点蛋白激酶 1 ( check point kinase 1 , CHEK1 )、 AURKA 共 5 个靶点为核心靶点。对分子对接得分进行热图分析,结果显示 CDK1 与这 6 个核心成分均有较好的结合活性(结合能均< − 5 kJ/moL ,图 4-B )。将上述 5 个靶点在肿瘤组织与正常组织之间的表达量差异进行分析,结果显示以上 5 个靶点在肝癌组织及正常组织中的表达均有较大差异(图 4-C )。
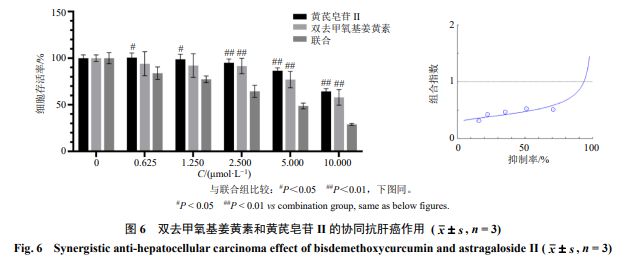
为了评价黄芪 - 莪术药对成分配伍的体外抗肿瘤协同作用,选择双去甲氧基姜黄素和黄芪皂苷 II 进行协同作用研究,通过 Chou-Talalay 数学模型进行协同作用效果评价 [27] 。结果如图 6 所示,与单独药物作用相比,联合组的细胞活力显著降低( P < 0.05 、 0.01 )。为了查明该组合是否起到加和作用或协同作用,使用 CompuSyn 软件进一步分析细胞活性数据,结果表明各浓度的双去甲氧基姜黄素和黄芪皂苷 II 在中位有效剂量(组合指数< 1 )时均表现出协同作用,其最佳协同剂量为 0.625 μmol/L 黄芪皂苷 II 和 0.625 μmol/L 双去甲氧基姜黄素。
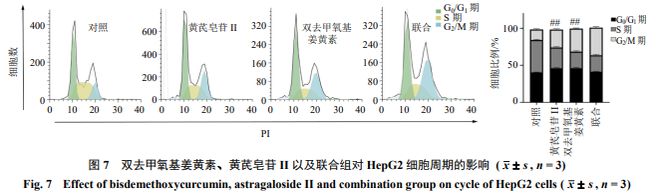
细胞周期检测结果显示,黄芪皂苷 II ( 5 μmol/L )和双去甲氧基姜黄素( 5 μmol/L )以及联合给药(黄芪皂苷 II 2.5 μmol/L +双去甲氧基姜黄素 2.5 μmol/L )处理 HepG2 细胞 24 h 后可导致细胞周期异常。如图 7 所示,与对照组比较,不同组别药物处理 HepG2 细胞 24 h 后,各组 G2/M 期的细胞比例 均升高。与单用黄芪皂苷 II 和双去甲氧基姜黄素组相比,联合组 G2/M 期细胞比例显著升高( P < 0.01 ),上述结果提示黄芪皂苷 II 与双去甲氧基姜黄素均能诱导 HepG2 细胞周期停滞于 G2/M 期,且联用效果更佳( P < 0.01 )。
古今医家多认为正气亏虚为肝癌的发病内因和前提,瘀血凝滞是肝癌发病的基本病理因素,正气不足、瘀血阻滞始终伴随着肝癌的发生、发展和转移[28] 。因此临床治疗肝癌常将黄芪、莪术等益气药与活血药配伍使用,不仅可辅助正气,同时能行气活血,两者兼顾,共凑扶正祛邪之效[11-13,29-30] 。
本研究利用生物信息学结合网络药理学与分子对接技术探究黄芪- 莪术药对治疗肝癌的活性成分、潜在靶点和信号通路,进而揭示其配伍机制。结果显示,黄芪- 莪术抗肝癌活性成分33 种,其中黄芪22 种、莪术12 种、两者共有成分1 种;对应抗肝癌靶点180 个,其中黄芪调节77 个、莪术调节14 个、两者共同调节89 个;KEGG 通路富集分析显示黄芪- 莪术药对调节抗肝癌通路31 条,其中黄芪调节20 条、莪术调节20 条、共同调节9 条。以上结果从成分、靶点、通路3 个方面揭示了黄芪、莪术配伍协同抗肝癌的科学内涵。
KEGG 通路结果显示黄芪- 莪术药对主要通过细胞周期、细胞衰老、p53 信号通路、细胞凋亡、代谢通路等发挥抗肝癌作用。其中细胞周期、p53 信号通路是与肿瘤发生发展密切相关的信号通路,在调控肝癌细胞周期、增殖、凋亡、细胞代谢等行为上发挥重要作用。p53 作为一种转录因子,通过调节其下游基因的表达来调控细胞周期阻滞、细胞衰老、DNA 修复和细胞凋亡等过程,p53 缺失不仅会引起细胞的增加和细胞存活率的提高,还会引起更具侵袭性的行为和基因组不稳定性的增加[31] 。p53 下游靶蛋白p21 和CDK2 调控细胞周期的进行,CDK2 与CCNA 、CCNE 相互作用可使Rb 蛋白磷酸化,从而促进细胞从G1 期进入S 期,p21 可以抑制其相互作用从而抑制细胞周期进程[32-33] 。
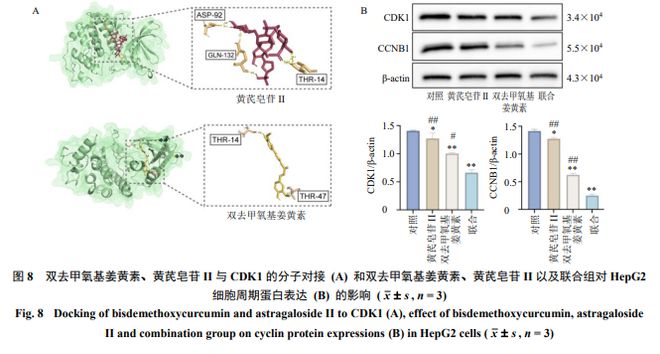
经筛选得到的 6 个核心成分(黄芪甲苷、黄芪皂苷 II 、芒柄花素、姜黄素、双去甲氧基姜黄素、莪术醇),均具有不同程度的抗肿瘤作用,其调控的5 个核心基因(CDK1 、CHEK1 、TOP2A 、AURKA 、AURKB ),在肿瘤发生发展过程中同样具有重要的调控作用。研究表明,AURK 是一类丝/ 苏氨酸激酶,龙8long8唯一官方网站可以通过干扰中心体、纺锤体以及染色体的功能影响细胞的有丝,AURKA 调节有丝早期中心体成熟,参与建立双极纺锤体,其功能的有效发挥离不开周期蛋白B 与CDK 复合物(cyclin B-CDK1 )的正常作用,活化的cyclin B-CDK1 可以使蛋白磷酸酶1 (protein phosphatase 1 ,PP1 )失活,PP1 可以抑制AURKA 活性[34] 。CDK1 是调控细胞周期的关键蛋白,CHEK1 为调控CDK 蛋白的上游蛋白,CHEK1 的磷酸化能够导致细胞周期因子25A/C (cell division cyclin 25A/C ,CDC25A/C )的磷酸化失活,从而抑制CDK1 进入有丝G2/M 期[35] 。分子对接结果显示核心成分(黄芪甲苷、黄芪皂苷 II 、芒柄花素、姜黄素、双去甲氧基姜黄素、莪术醇)与核心靶点(CDK1 、CHEK1 、TOP2A 、AURKB 、龙8long8唯一官方网站AURKA )结合能较强,可能存在较好的结合活性。研究发现,芒柄花素通过环氧合酶-2/ CCND 轴将人肝癌Bel-7402 细胞和HepG2 细胞阻滞于G0/G1 期[36-37] ;莪术醇可以阻滞HepG2 细胞于G1 期[38] ;黄芪甲苷能够上调具有低转移潜能和高转移潜能的人肝癌Huh7 细胞和人肝癌MHCC97-H 细胞中E- 钙黏蛋白的蛋白水平并促进其在细胞膜上积累,使得细胞间连接更加紧密从而降低转移扩散能力;姜黄素能够通过激活Huh7 细胞内死亡受体介导的通路诱导凋亡[39] ;且黄芪甲苷与姜黄素联用对血管生长因子(vascular endothelial growth factor ,VEGF )、基质金属蛋白酶2 (matrix metallopeptidase 2 ,MMP2 )、成纤维细胞生长因子-2 (fibroblast growth factor-2 ,FGF-2 )、肝细胞生长因子(hepatocyte growth factor ,HGF )以及血栓形成相关因子组织因子(tissue factor ,TF )和凝血因子 VII 有协同抑制作用[40] 。
通过体外细胞实验验证了黄芪 - 莪术药对6 个核心成分对HepG2 细胞的增殖均具有明显的抑制作用。协同作用分析结果显示,黄芪中的黄芪皂苷 II 和莪术中的双去甲氧基姜黄素配伍有协同作用,其最佳协同剂量为黄芪皂苷 II 0.625 μmol/L 、双去甲氧基姜黄素0.625 μmol/L 。2 个成分配伍使用可协同增效抑制周期调控蛋白CDK1 和CCNB1 的表达,进而诱导HepG2 细胞停滞于G2/M 期。
本研究基于生物信息学数据,结合网络药理学方法与分子对接技术及细胞实验证明了黄芪、莪术配伍能够通过多成分、多靶点、多通路在肝癌治疗中发挥协同作用,为更准确寻找、确认和优化黄芪、莪术发挥抗肝癌效应的有效成分与靶点的作用,推动临床应用提供新的见解。
来 源:鲍 宁,陈子超,刘名玉,赵春芹,李 肖,张 振.整合生物信息学与实验验证解析黄芪-莪术药对抗肝癌配伍机制 [J]. 中草药, 2024, 55(1): 114-126.